Transfundierende Ärzte
Hämotherapie
DasTransfusionsgesetz legt die in Deutschland gültigen Vorgaben für die Transfusion von Blutpräparaten fest.
Die Richtlinie zur Gewinnung von Blut und Blutbestandteilen und zur Anwendung von Blutprodukten (Richtlinie Hämotherapie) gemäß den §§ 12a und 18 des Transfusionsgesetzes beschreibt die Einzelheiten zur klinischen Hämotherapie.
Die Querschnitts-Leitlinien (BÄK) zur Therapie mit Blutkomponenten und Plasmaderivaten erläutern den klinische Einsatz von Blutprodukten.
Die Voten des Arbeitskreises Blut legen die Verfahrensweisen bei der Herstellung und Anwendung von Blutpräparaten fest.
Die Verordnung über die Anwendung der Guten Herstellungspraxis bei der Herstellung von Arzneimitteln und Wirkstoffen und über die Anwendung der Guten fachlichen Praxis bei der Herstellung von Produkten menschlicher Herkunft gibt die einzuhaltenden Bestimmungen für Hersteller von Blutpräparaten an.
Votum Nr. 48 des Arbeitskreises Blut erläutert das Verfahren zur Rückverfolgung (Look Back) gemäß § 19 Transfusionsgesetz.
Bei Verdacht der Übertragung einer Hepatitis B-, Hepatitis C- oder HIV-Infektion durch Blutprodukte ist der Transfusionsverantwortliche des Klinikums einzuschalten.
Weiterführende Informationen:
Gesetz zur Verhütung und Bekämpfung von Infektionskrankheiten beim Menschen
Richtlinien über die ärztliche Betreuung während der Schwangerschaft und nach der Entbindung (Mutterschafts-Richtlinien) enthält Informationen zu immunhämatologischen Untersuchungen während der Schwangerschaft und Festlegungen zur Rhesusprophylaxe
Unterlagen zur Transfusion
Transfusionsmedizinische Dienstanweisung, QM-Handbuch
- Transfusionsmedizinischen Dienstanweisung für das Universitätsklinikum Rostock (Nexus Curator Dok.-Nr. 68695)
- Qualitätsmanagement-Handbuch für die klinische Anwendung von Blutprodukten und Plasmaderivaten (Nexus Curator Dok.-Nr. 66174)
Schulungsunterlagen
- Anleitung Nutzung SAP: Abrufen von Patienteninformationen und Anlegen von Klinischen Aufträgen & Konsilen
Download Anforderungsscheine
- Blutbank (Blutprodukte und erythrozytenserologische Laborleistungen)
- präoperative Eigenblutspende
Gebrauchs- und Fachinformationen
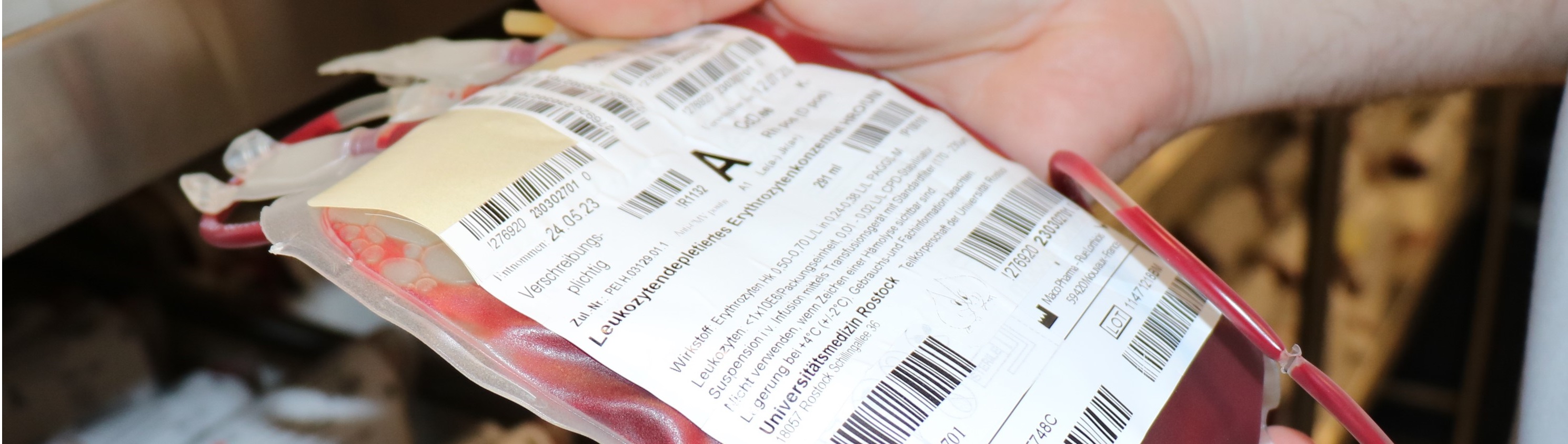
Die Angaben dieser Gebrauchs- und Fachinformation werden stets neuen Erkenntnissen angepasst und sollten vor Gebrauch eines jeden Blutbeutels beachtet werden.
- Gefrorenes Frischplasma (Apherese)
- Gefrorenes Frischplasma (VB)
- Lyophilisiertes Plasma (Apherese)
- Leukozytendepletiertes Erythrozytenkonzentrat/bestrahlt
- Leukozytendepletiertes Erythrozytenkonzentrat
- Pool-Thrombozytenkonzentrat, leukozytendepletiert
- Leukozytendepletiertes Thrombozytapheresekonzentrat/bestrahlt
- Leukozytendepletiertes Thrombozytapheresekonzentrat
Bestrahlungsindikationen
Die für die UMR geltenden Bestrahlungsindikationen entsprechen den "Querschnitts-Leitlinien zur Therapie mit Blutkomponenten und Plasmaderivaten" der Bundesärztekammer. Diese sollten stets beachtet werden.

Abklärung Verdacht auf Transfusionsreaktion
Für die Meldung einer Transfusionsreaktion verwenden Sie die Funktion "Klinischer Auftrag" im SAP (Reiter Transfusionsmedizin).
Füllen Sie das Meldeformular vollständig aus und senden es gemeinsam mit den korrekt gefüllten Blutproben zu uns.
Untersuchungsmaterial
- 7,5 ml Nativblut ohne gerinnungshemmende Zusätze
- 7,5 ml EDTA-Blut
- ggf. eine Patienten-Blutprobe vor Transfusion
Dokumentation der Anwendung von Blutprodukten
gemäß §14 Transfusionsgesetz
In der UMR wird die produkt- bzw. chargenbezogene Dokumentation von zellulären Blutprodukten und gefrorenem Frischplasma durch die Zentral-Apotheke bis zur Kostenstelle der Station / Ambulanz sichergestellt.
In den Einrichtungen der Krankenversorgung (Station, Ambulanz, OP-Bereich) ist diese Dokumentation fortzusetzen. Zu einem späteren Zeitpunkt muss die komplette Zuordnung aller verabreichten dokumentationspflichtigen Präparate zum Patienten ersichtlich sein.
(Weitere Einzelheiten siehe Abschnitt 4.10 Transfusionsmedizinische Dienstanweisung)
patientenbezogene Produktdokumentation
Folgende Dokumente stehen zur Verfügung:
Einlegeblatt Dokumentation der Anwendung dokumentationspflichtiger Plasmaproteine
Einlegeblatt Dokumentation der Anwendung von gefrorenem Frischplasma (Depot)
Produktdokumentation von Erythrozyten-Konzentraten erfolgt entweder
- analog, über Service-Klebeetiketten in der Krankenakte
oder:
- elektronisch, über scannen der grün markierten Barcodes (Konservennummer):
Erstellung von Blutgruppen-Befunden außerhalb der regulären Dienstzeit
Erstellung von Befunden nur bei unmittelbarer Transfusion:
- täglich zwischen 19:00 Uhr und 07:00 Uhr
- an Wochenenden und Feiertagen
Dies sind vorläufige Befunde. Endgültige Befunde erhalten Sie am nächsten Werktag.
Ersetzen Sie den vorläufigen Befund immer durch den endgültigen Befund in den Patientenunterlagen!